La miocardiopatía hipertrófica (hipertrofia inexplicada del VI ≥15 mm) afecta hasta al 0.5% de la población; entre el 30-60% de los pacientes portadores presentan una variante genética patogénica o probablemente patogénica (PP), constituyendo así la miocardiopatía genética más frecuente. Tradicionalmente se considera que la correlación genotipo-fenotipo es pobre, no obstante se ha invertido mucho esfuerzo en los últimos años para lograr dilucidar esta correlación y así perfeccionar la precisión diagnóstica.
Si bien la forma más frecuente de presentación de la MCH sarcomérica es la afección septal asimétrica, principalmente con morfología de septum reverso, la MCH puede presentarse con hipertrofia de cualquiera de los segmentos de VI, e incluso de VD. Este estudio publicado recientemente en la revista EHJ Cardiovascular Imaging tiene como objetivo trazar una relación entre los patrones de hipertrofia y las variantes genéticas patogénicas. Para ello se analizaron 392 pacientes habitantes de China con diagnóstico de MCH, mediante ecocardiografía y análisis genético con técnica de secuenciación de exoma completo. El 68% eran hombres, la media de espesor máximo septal era de 19.9 ± 5 mm, y el 27% presentaba MCH con obstrucción del tracto de salida en reposo. Aproximadamente el 13% de los pacientes presentaban hipertrofia del ventrículo derecho (≥6 mm) además de VI. El 18% de los pacientes mostraron disfunción sistólica del VI, y el 9% del VD.
Se identificaron 67.3% pacientes con mutaciones patogénicas (o PP): proteína C fijadora de miosina (MYBPC3) 32.2%, cadena pesada de miosina 7 (MYH7) 19.7%, troponina I3 (TNNI3) 6%, troponina T2 (TNNT2) 4.5%, alpha kinase 3 (ALPK3) 3,7%, tropomiosina 1 (TPM1) 3,7%, y obscurina (OBSCN) y titina (TTN) 3,4% cada uno. 67% eran variantes missense, y se observó una alta proporción de mutaciones en heterocigosis compuesta (23.5%).
Los pacientes con genotipo positivo eran más jóvenes, presentaban fenotipos más severos, y más hipertrofia de VD, más marcado aún en pacientes con mutaciones truncantes.
Las mutaciones en MYH7, MYBPC3 y otros genes sarcoméricos o de miofilamento (TNNI3, TPM1 y TNNT2) se encontraron en hipertrofias de pared anterior, septum y pared lateral del VI. En contraste, la hipertrofia asociada a las variantes en ALPK3 se observó principalmente en la región apical, mientras que los patrones de hipertrofia relacionados con las mutaciones de TTN y OBSCN mostraron una distribución uniforme en todo el miocardio. La Figura 1 esquematiza en el mapa polar ecocardiográfico la relación entre los sitios de hipertrofia y las variantes patogénicas. No obstante, con excepción de una mayor frecuencia de OTSVI y mayor relación septal-pared posterior en pacientes portadores de MYH7, no se observaron mayores diferencias fenotípicas entre las dos mutaciones sarcoméricas más frecuentes de la MCH (MYH7 y MYBPC3), haciéndolas fenotípicamente indistinguibles. El análisis multivariado mostró que cuatro parámetros eran predictores independientes de una prueba genética positiva: la menor edad al momento del diagnóstico, la dimensión del seno aórtico, la relación septal-pared posterior, y el diámetro anteroseptal medial, siendo este último el de mayor fuerza de relación (OR 2.18).
Estos patrones de correlación genotipo-fenotipo determinan un novedoso concepto de relación “gen-ecocardiografía”, lo cual resulta valioso a la hora de mejorar la precisión y eficiencia del estudio y asesoramiento genético en la MCH.
Bibliografía
Nianwei Zhou, Haobo Weng, Weipeng Zhao, Lu Tang, Zhendan Ge, Fangyan Tian, Fangmin Meng, Cuizhen Pan, Xianhong Shu, Gene-echocardiography: refining genotype–phenotype correlations in hypertrophic cardiomyopathy, European Heart Journal – Cardiovascular Imaging, 2023;, jead200, https://doi.org/10.1093/ehjci/jead200
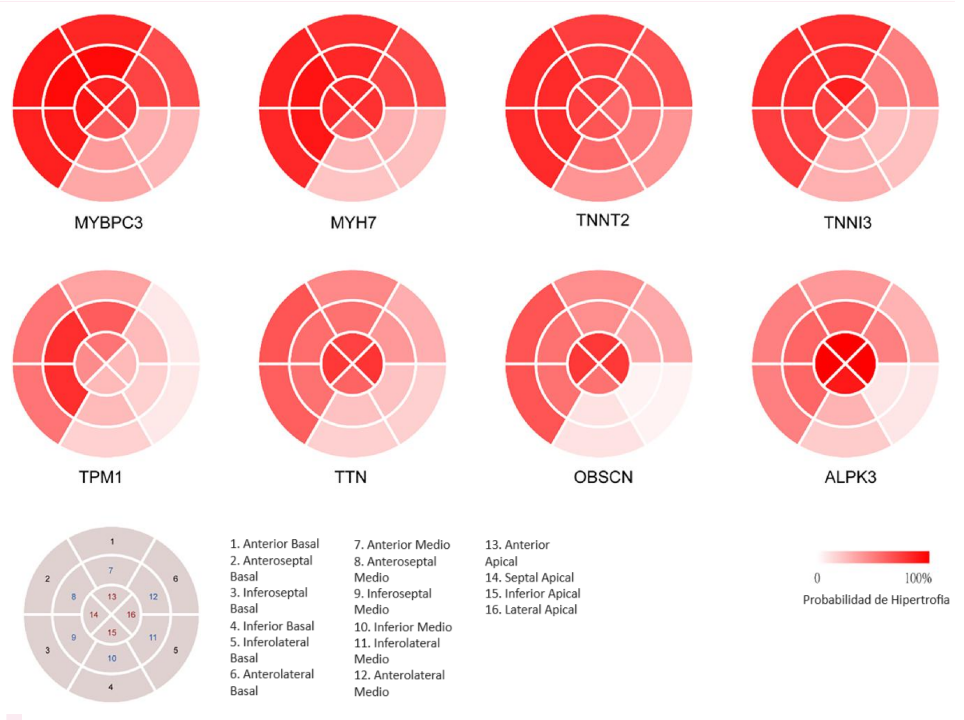
FIGURA 1: Correlación gen-fenotipo en MCH. El mapa polar representa los segmentos ecocardiográficos. La barra de color marca la probabilidad de hipertrofia de cada segmento según la correlación genética.






